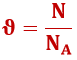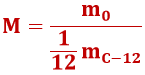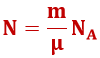Ainehulk. Mass. Tihedus
Ainehulk on füüsikaline suurus, mis iseloomustab ainekoguses sisalduvate molekulide arvu.
Ainehulga mõõtühikuks on 1 mool (1 mol). Mool on SI põhiühik! 1 mool on selline ainehulk, milles molekulide arv võrdub 0,012 kg süsinik-12 aatomite arvuga. 1 mool mistahes ainet sisaldab ühepalju molekule – seda arvu nimetatakse Avogadro arvuks:
Keha ainehulk (ϑ – kreeka täht nüü) võrdub selle keha molekulide arvu (N) ja Avogadro arvu (NA) suhtega:
Sulle võivad huvi pakkuda need õppematerjalid:
8. klassi matemaatika teooriavideod
xy-koordinaatsüsteem
INETU PARDIPOEG. Muinasjutt kuulamiseks
Harjutusülesandeid matemaatika riigieksamiks
VAPPER TINASÕDUR. Muinasjutt kuulamiseks
Ruumilised kujundid
Häälikute pikkused
Ruutvõrrand
Eesti keele grammatika gümnaasiumile: kokku- ja lahkukirjutamine
Urme Raadik ja Sille Jõgeva. Omavahelised suhted
Ratsionaalavaldised
Eesti keele grammatika gümnaasiumile: algustäheortograafia
Ruutjuur, tehted ruutjuurtega
Peastarvutamine eelkoolile
Harjuta eesti keelt A2-B1. Kuulamine
Jane Snaith. Traumateadlik kool
Ионы
Ehkki oleme näidanud, et keha mass on füüsikaline suurus, mis iseloomustab keha inertsust (inertne mass) ja/või võimet astuda gravitatsioonilisse vastastikmõjusse (raske mass), on selle abil võimalik kirjeldada ka kehas sisalduva aine kogust.
Kuna molekulide ja aatomite massid on väga väikesed (suurusjärgus 10-24kg), siis kasutatakse nende kirjeldamisel absoluutväärtuste asemel hoopis suhtelist väärtust – molekulmassi – aine molekulmass (M) iseloomustab mitu korda erineb tema molekuli mass (m0) 1/12 süsinik-12 molekuli massist ehk aatommassiühikust (1u = 1/12mC-12=1,6605402∙10-27kg ≈ 1,66∙10-27kg):
NB! Molekulmass on ühikuta suurus.
Teades, et ühes moolis sisaldub alati Avogadro arv osakest (NA) ning ühe osakese massi (m0), saame leida ühe mooli vastava aine massi – molaarmassi (μ – kreeka täht müü):
Molaarmassi ühikuks on kilogrammi mooli kohta (1 kg/mol = 1 kg∙mol-1)
Seega on suvalise ainekoguse mass (m) leitav ainehulga (ϑ) ja molaarmassi (μ) kaudu:
ning suvalise massiga ainekoguses sisalduvate osakeste hulka võimalik leida valemist: