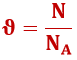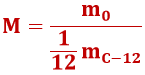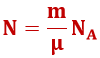Ainehulk. Mass. Tihedus
Ainehulk on füüsikaline suurus, mis iseloomustab ainekoguses sisalduvate molekulide arvu.
Ainehulga mõõtühikuks on 1 mool (1 mol). Mool on SI põhiühik! 1 mool on selline ainehulk, milles molekulide arv võrdub 0,012 kg süsinik-12 aatomite arvuga. 1 mool mistahes ainet sisaldab ühepalju molekule – seda arvu nimetatakse Avogadro arvuks:
Keha ainehulk (ϑ – kreeka täht nüü) võrdub selle keha molekulide arvu (N) ja Avogadro arvu (NA) suhtega:
Sulle võivad huvi pakkuda need õppematerjalid:
Lahused
Tähestik, tähestikuline järjekord, häälikute jagunemine
Harjutusülesandeid matemaatika riigieksamiks
Toivo Niiberg. Õpetaja positiivne enesekehtestamine lapsevanemaga
Eesti keele grammatika kordamine 7. klassile
Eesti keele grammatika kordamine 8. klassile
Urme Raadik ja Sille Jõgeva. Omavahelised suhted
Liitmine 10 piires
Kirjalik liitmine
Numbrilised seosed
Ehkki oleme näidanud, et keha mass on füüsikaline suurus, mis iseloomustab keha inertsust (inertne mass) ja/või võimet astuda gravitatsioonilisse vastastikmõjusse (raske mass), on selle abil võimalik kirjeldada ka kehas sisalduva aine kogust.
Kuna molekulide ja aatomite massid on väga väikesed (suurusjärgus 10-24kg), siis kasutatakse nende kirjeldamisel absoluutväärtuste asemel hoopis suhtelist väärtust – molekulmassi – aine molekulmass (M) iseloomustab mitu korda erineb tema molekuli mass (m0) 1/12 süsinik-12 molekuli massist ehk aatommassiühikust (1u = 1/12mC-12=1,6605402∙10-27kg ≈ 1,66∙10-27kg):
NB! Molekulmass on ühikuta suurus.
Teades, et ühes moolis sisaldub alati Avogadro arv osakest (NA) ning ühe osakese massi (m0), saame leida ühe mooli vastava aine massi – molaarmassi (μ – kreeka täht müü):
Molaarmassi ühikuks on kilogrammi mooli kohta (1 kg/mol = 1 kg∙mol-1)
Seega on suvalise ainekoguse mass (m) leitav ainehulga (ϑ) ja molaarmassi (μ) kaudu:
ning suvalise massiga ainekoguses sisalduvate osakeste hulka võimalik leida valemist: