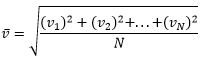Ideaalse gaasi rõhk
Ideaalne gaas on reaalse gaasi lihtsustatud mudel kus: (1) gaasimolekulid loetakse punktmassideks; (2) molekulide põrked anuma seintega on absoluutselt elastsed; (3) molekulide vahel puudub vastastikmõju ehk teiste sõnadega: (1) molekulide ruumala jäetakse arvestamata, (2) anuma seinaga põrkudes muutub ainult molekuli kiiruse suund, suurus jääb samaks ning (3) gaasimolekulide vahel ei mõju tõmbe- ega tõukejõude.
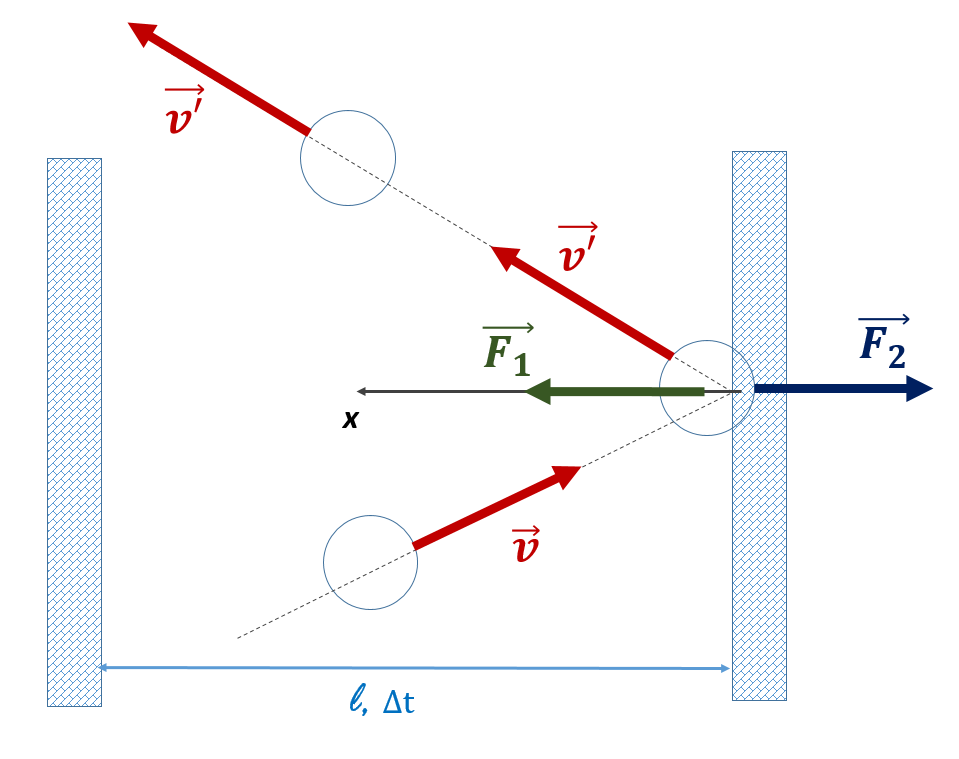
Ideaalse gaasi molekulid põrkuvad anuma seintega, nende liikumishulk (impulss) muutub ning seetõttu mõjutavad gaasimolekulid seina mingi jõuga.
Rõhk iseloomustab jõu (mida gaasimolekulid põrkudes seinaga avaldavad) mõju pinnaühikule:
Millest sõltub gaasimolekulide poolt anuma seintele avaldatav jõud?
Sulle võivad huvi pakkuda need õppematerjalid:
Ruutvõrrandi mõiste, ruutvõrrandi lahendivalem, ruutvõrrandi liigid
Ratsionaalavaldised
Tutvus keemiaga
Reesi Kuslap ja Kristiine Kurema. Kuidas õhinaga õpetada ehk mismoodi innustada õpilasi õppima?
Silbitamine algklassidele
Ruutjuur, tehted ruutjuurtega
Атомы и молекулы
Растворы
Eesti keele grammatika kordamine 7. klassile
HANS JA GRETE. Muinasjutt kuulamiseks
Harjuta eesti keelt A2-B1
Peastarvutamine eelkoolile
Eesti keele grammatika gümnaasiumile: kokku- ja lahkukirjutamine
Eesti keele grammatika gümnaasiumile: täheortograafia
(1) osakeste liikumiskiirusest: mida kiiremini osake liigub à seda rohkem muutub põrkudes osakese liikumishulk à seda suurem on seinale avaldatav jõud à seda suurem on rõhk
(2) osakese massist: mida suurem on osakese mass à seda suuremat mõju ta seinaga põrkudes avaldab à seda suurem on jõud à seda suurem on rõhk;
(3) osakeste kontsentratsioonist: mida rohkem on osakesi ruumalaühikus à seda rohkem põrkeid à seda suurem jõud seinale mõjub à seda suurem on rõhk.
Ülaltoodut arvestades saab näidata, et ideaalse gaasi molekulide poolt anuma ja seintele avaldatav rõhk, mis on kõikides suundades ühesugune, on arvutatav valmist:
kus: p – ideaalse gaasi poolt anuma seintele avaldatav rõhk, n – molekulide kontsentratsioon n=N/V (N– osakeste arv anumas; V – anuma ruumala), mõõdetühikuks 1m-3 – loe osakest kuupmeetri kohta, m0 – molekuli mass ning ![]() – molekulide ruutkeskmine kiirus, mis sisuliselt on kõikide gaasimolekulide kiiruste ruutude aritmeetiline keskmine ning sõltub sellest millise gaasiga on tegu ning eelkõige sellest, milline on selle gaasi temperatuur:
– molekulide ruutkeskmine kiirus, mis sisuliselt on kõikide gaasimolekulide kiiruste ruutude aritmeetiline keskmine ning sõltub sellest millise gaasiga on tegu ning eelkõige sellest, milline on selle gaasi temperatuur:
ANIMATSIOON: