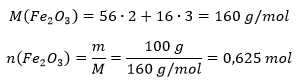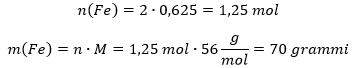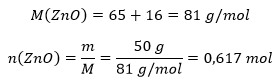Reaktsiooni saagis
Sünteesides keemilisi aineid, esinevad reaktsioonis alati kaod – reaktsioon ei kulge lõpuni, osa aineid jääb nõude külge jne. Seda, kui palju ainet saadakse reaktsiooni käigus kätte võrreldes teoreetilise kogusega näitab reaktsiooni saagis. Enamasti väljendatakse seda protsentides.
Arvutusülesanne 1: Milline on reaktsiooni saagis, kui 100 grammi raud(III)oksiidi redutseerimisel saadi 50 grammi puhast rauda?
Lahendus: Kirjutame välja reaktsioonivõrrandi. Antud ülesande korral pole oluline, millist redutseerijat kasutati, seega kirjutame välja võrrandi näiteks vesinikuga.
Fe2O3 + 3H2 = 2Fe + 3H2O
Leiame, mitu mooli raud(III)oksiidi alguses oli:
Sulle võivad huvi pakkuda need õppematerjalid:
Ioonid
Атомы и молекулы
Lahused
Знакомство с химией
Ионы
Tutvus keemiaga
Oksüdatsiooniaste
Aatomid ja molekulid
Растворы
Vastavalt reaktsioonivõrrandile, tekib rauda kaks korda rohkem (raua ees on kordaja kaks ning raud(III)oksiidi ees üks). Võrrandi järgi tekkinud raua mass on seega:
Teoreetiline kogus rauda, mis saaks 100 grammist raud(III)oksiidist tekkida on 70 grammi. Tegelikult saadi 50 grammi, seega on reaktsiooni saagis p:
Vastus: Reaktsioonisaagis on 71,4%
Arvutusülesanne 2: Mitu grammi tsinki saadakse 50 grammi tsinkoksiidi redutseerimisel süsinikuga, kui reaktsiooni saagis on 80%?
Lahendus: Kirjutame reaktsioonivõrrandi
2ZnO + C = 2Zn + CO2
Leiame tsinkoksiidi hulga:
Võrrandi järgi tekib tsinki sama palju (kordajad on tsingi ja tsinkoksiidi ees samad), seega oleks tekkinud tsingi mass:
See on teoreetiline kogus, kuna saagis on 80%, siis tegelikult saadud tsingi mass on:
Vastus: Tsinki saadi reaktsiooni käigus 32,1 grammi.