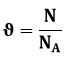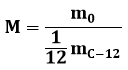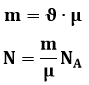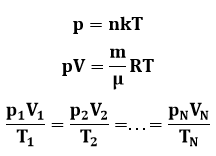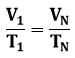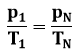Soojusnähtused
Ainehulk:
kus ϑ – ainehulk, N molekulide arv kehas, NA=6,02∙1023 mol-1 – Avogadro arv
Molekulmass:
kus M – molekulmass (ühikuta), m0 – aine molekuli mass (kg); ![]() – süsinik-12 aatomi mass (kg)
– süsinik-12 aatomi mass (kg)
Sulle võivad huvi pakkuda need õppematerjalid:
Ruumilised kujundid
Silbitamine algklassidele
Lahused
Eesti keele grammatika gümnaasiumile: kokku- ja lahkukirjutamine
Eesti keele grammatika kordamine 7. klassile
Tasandilised kujundid
Eesti keele grammatika gümnaasiumile: numbrite kirjutamine
Eesti keele grammatika kordamine 9. klassile
Haridustreff 2023 loengud
Häälikute pikkused
Jäätmed pole kõigest prügi
Liitmine 10 piires
Peastarvutamine eelkoolile
Urme Raadik ja Sille Jõgeva. Omavahelised suhted
Funktsioonide graafikud
Molaarmassi:
kui μ – molaarmass (kg/mol); NA=6,02∙1023 mol-1 – Avogadro arv; m0 – molekuli mass (kg)
Ainekoguse mass, osakeste arv selles:
kus m – ainekoguse mass (kg), ϑ – ainehulk (mol), μ – molaarmass (kg/mol), N – osakeste arv ainekoguses, NA=6,02∙1023 mol-1 – Avogadro arv
Ideaalgaasi molekulide keskmine kineetiline energia (temperatuuri definitsioonvalem):
kus ![]() – gaasimolekulide keskmine kineetiline energia = molekulide kineetiliste energiate aritmeetiline keskmine (J), k = 1,3806578∙10-23 J/K ≈ 1,38∙10-23 J/K – Boltzmann’i konstant ning T – keha temperatuur (K).
– gaasimolekulide keskmine kineetiline energia = molekulide kineetiliste energiate aritmeetiline keskmine (J), k = 1,3806578∙10-23 J/K ≈ 1,38∙10-23 J/K – Boltzmann’i konstant ning T – keha temperatuur (K).
Ideaalse gaasi rõhk:
kus: p – ideaalse gaasi poolt anuma seintele avaldatav rõhk (Pa), n – molekulide kontsentratsioon (m-3) – n=N/V (N – osakeste arv anumas; V – anuma ruumala – m3), ![]() – molekulide ruutkeskmine kiirus (m2/s2).
– molekulide ruutkeskmine kiirus (m2/s2).
Ideaalse gaasi olekuvõrrand:
kus p – gaasi rõhk (Pa), n – osakeste kontsentratsioon (n-3), T – gaasi temperatuur (K), k = 1,38∙10-23 J/K – Boltzmann’i konstant, V – gaasi ruumala (m3), m – gaasi mass (kg), μ – gaasi molaarmass (kg/mol), R = NA∙k = 8,314510 J/(mol∙K) ≈ 8,31 J/(mol∙K) – universaalne gaasikonstant; p1, V1, T1 – on gaasi rõhk, ruumala ja temperatuur ühes olekus, pN, VN ja TN – aga sama gaasikoguse rõhk, ruumala ja temperatuur mingis teises olekus.
Boyle’ – Mariotte’i seadus (isotermiline protsess):
kus p1, V1,– on gaasi rõhk (Pa), ruumala (m3) ühes olekus, pN, VN N – aga sama gaasikoguse rõhk ja ruumala mingis teises olekus.
Gay-Lussac’i seadus (isobaariline protsess):
kus V1, T1,– on gaasi ruumala (m3) ja temperatuur (K) ühes olekus, VN, TN – aga sama gaasikoguse temperatuur ja ruumala mingis teises olekus.
Charles’i seadus (isohooriline protsess):
kus p1, T1,– on gaasi rõhk (Pa) ja temperatuur (K) ühes olekus, pN, TN – aga sama gaasikoguse rõhk ja temperatuur mingis teises olekus.