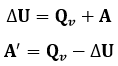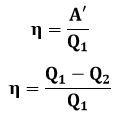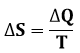Termodünaamika alused
Soojushulk keha soojenemisel/jahtumisel:
kus Q – soojushulk (J), m – keha mass (kg) ning ΔT = T2 – T1 – temperatuuri muutus (T2 ja T1 on soojusülekande käigus soojenenud/jahtunud keha vastavalt lõpp- ja algtemperatuurid – K), c – on keha materjali iseloomustav erisoojus (J/(kg∙K). NB! võib kasutada ka Celsiuse kraade.
Sulle võivad huvi pakkuda need õppematerjalid:
Tundetarkus lastele. ÜLLATUS
Tundetarkus lastele. HIRM
Harjutamine teeb meistriks: eesti keele käänded
Растворы
Tähestik, tähestikuline järjekord, häälikute jagunemine
Õpime tähti. D-täht
Harjuta eesti keelt A2-B1. Kuulamine
Знакомство с химией
Ruutvõrrandi abil lahenduvad tekstülesanded
Õpime tähti. Ä-täht.
Tundetarkus lastele. RÕÕM
Algebralised murrud
Rahvakalender lastele: VOLBRIPÄEV
Soojuslik tasakaal soojusvahetuse korral suletud süsteemis:
kus Q1, Q2 … QN on erinevate suletud süsteemi kuuluvate soojusvahetuses osalevate kehade soojushulgad – J.
Termodünaamika I printsiip:
kus ΔU – isoleerimata termodünaamilise süsteemi siseenergia muut, Qv – süsteemile soojusülekandel väliskeskkonna poolt antud soojushuk, A – süsteemiga tehtud mehaaniline töö, A’ – süsteemi poolt tehtav mehaaniline töö (kõik J).
Ideaalse gaasi töö isobaarilisel paisumisel:
kus A’ – gaasi poolt tehtav töö (J); p – gaasi rõhk (Pa); ΔV = V2 – V1- gaasi ruumala muutus – V2 – lõppruumala, V1 – algruumala (m3)
Soojusmasina poolt tehtav töö:
kus A’ – soojusmasina poolt tehtud töö, Q1 – soojendilt saadud soojushulk, Q2 – jahutile antud soojushulk (kõik J)
Soojusmasina kasutegur:
kus η – kasutegur (ühikuta või %), A’ – soojusmasina poolt tehtud töö, Q1 – soojendilt saadud soojushulk, Q2 – jahutile antud soojushulk (kõik J)
Entroopia muutus (isotermilises protsessis):
kus ΔS süsteemi entroopia muutus (J/K), Q – süsteemi siseenergia muutus – soojushulk (J) ning T – süsteemi absoluutse temperatuuri (K).
Märkasid viga? Anna sellest teada ja teeme TaskuTarga koos paremaks!