Faasisiirded ja siirdesoojused
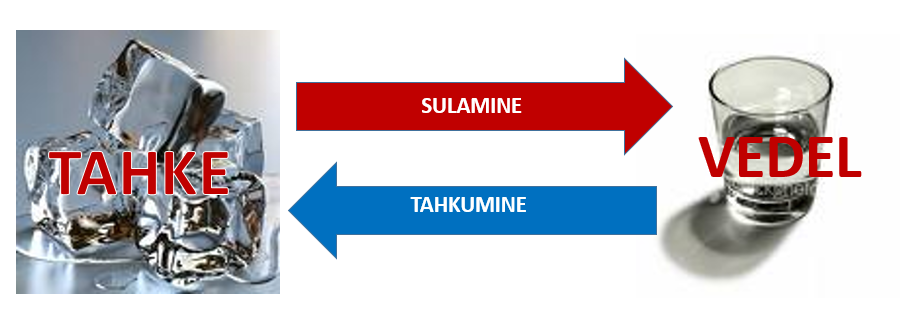
Sulamine-tahkumine
Sulamine on faasisiire tahkest olekust vedelasse, tahkumine sellele vastupidine siire.
Tahkumisel toimuvad muutused aineosakestega sulamisele vastupidises suunas.
Iga aine jaoks on olemas kindel temperatuur – sulamistemperatuur, mille juures ta muutub tahkest olekust vedelaks. Aine tahkub samal temperatuuril kui ta sulab
Sulle võivad huvi pakkuda need õppematerjalid:
Üksliikmed, hulkliikmed ja tehted nendega
Eesti keele grammatika kordamine 4. klassile
Rahvakalender lastele: VOLBRIPÄEV
Õpime tähti. Õ-täht
Kell ja kellaaeg
Aatomid ja molekulid
Ruutjuur, tehted ruutjuurtega
Reesi Kuslap ja Kristiine Kurema. Kuidas õhinaga õpetada ehk mismoodi innustada õpilasi õppima?
Ruutvõrrand
Õpime tähti. I-täht
Eesti keele grammatika kordamine 6. klassile
Õpime tähti. M-täht
Minni Aia-Utsal. Tõhusad enesekohased ja sotsiaalsed oskused
Häälikute pikkused
Sulamise/tahkumise ajal keha temperatuur ei muutu ehkki keha saab/annab selles protsessis pidevalt energiat – sulatamiseks kulunud energia läheb molekulide korrapära lõhkumiseks ja nende liikuvuse suurendamiseks. Tahkumisel vabaneva energia saame molekulide korrapära suurenemisest ja liikuvuse vähenemisest.
Keha sulatamiseks vajalik energiakogus (kehale antav soojushulk Q) on võrdeline keha massiga (m) ning sõltub keha materjalist:
Soojushulka, mis on vajalik 1 kg antud aine sulatamiseks tema sulamistemperatuuril nimetatakse aine sulamissoojuseks (λ – lamda)
Sulamissoojust mõõdetakse džaulides kilogrammi kohta 1 J/kg.
Kui 1 kilogrammi sulamistemperatuuril oleva keha sulatamiseks kulub 1J energiat, on selle keha materjali sulamissoojus 1 J/kg. Tahkumisel vabaneb sama palju soojust kui kulub sama koguse aine sulatamiseks:
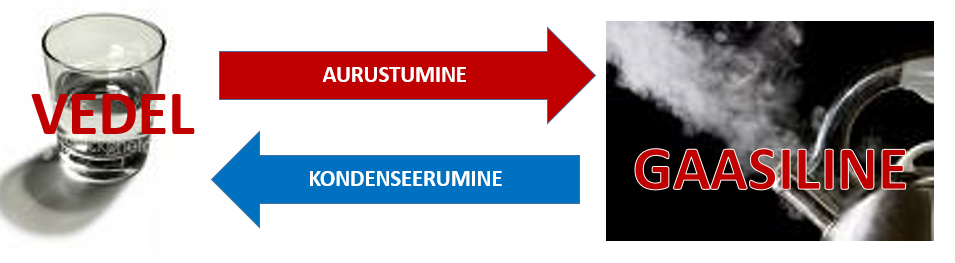
Aurustumine-kondenseerumine
Aurustumine on faasisiire vedelast olekust gaasilisse, kondenseerumine sellele vastupidine siire.
Vedeliku aurustumine ja kondenseerumine toimub alati vedeliku pinnal. Aurumisel väljuvad vedeliku pinnalt kiiremini liikuvad – suurema energiaga vedeliku molekulid. Tänu sellele aurustumisel vedeliku siseenergia (ja ka temperatuur) väheneb. Kondenseerumisel haaratakse aeglasemad gaasimolekulid (mis aga on kiiremad kui vedeliku omad) vedelikku ning tulemuseks on siseenergia suurenemine ning temperatuuri tõus.
Aurumise kiirus sõltub järgmistest teguritest:
- Vedeliku temperatuurist – mida kõrgem on temperatuur, seda kiiremini vedeliku molekulid liiguvad, seda rohkem on ennast lahti rebivaid osakesi – seda kiiremini vedelik aurub.
- Vedeliku pindalast – mida suurem on pindala, seda rohkem kiiremini liikuvaid vedeliku molekule saavad ennast lahti rebida – seda kiiremini vedelik aurub.
- Gaasi liikumisest vedeliku pinna kohal – kui vedelikust aurustunud gaas jääb vedeliku pinna kohale (õhk ei liigu), siis võidakse osad, aeglasemalt liikuvad gaasimolekulid tagasi vedelikku tõmmata. Mida kiiremini gaas vedeliku kohal liigub, seda kiiremini vedelik aurustub.
- Vedeliku koostisest – osades vedelikes on molekulide vahelised jõud tugevamad (molekulid asuvad teineteisele lähemal) – sellised vedelikud aurustuvad halvemini kui vedelikud, mille osakaste vaheline vastastikmõju on nõrgem.
Keemine on selline vedeliku aurustumine, mis toimub kindlal temperatuuril – keemistemperatuuril – kogu vedeliku ruumala ulatuses. Keemistemperatuur on seotud keeva vedeliku ainega – erinevatel ainetel on erinev keemistemperatuur. Samuti sõltub keemistemperatuur vedelikule atmosfääri poolt avaldatavast rõhust – mida kõrgem on rõhk, seda kõrgem on vedeliku keemistemperatuur.
Keemise ajal vedeliku temperatuur ei muutu ehkki vedelik saab kogu aeg energiat juurde.
Vedeliku keetmiseks kulunud energia läheb molekulide korrapära vähendamiseks ja nende liikuvuse suurendamiseks.
Vedeliku aurustamiseks keemis- või muul jääval temperatuuril vajalik energiakogus (soojushulk Q) on võrdeline vedeliku massiga (m) ning sõltub vedeliku materjalist:
Soojushulka, mis on vajalik 1 kg antud aine aurustamiseks tema keemistemperatuuril nimetatakse vedeliku keemissoojuseks (L).
Keemissoojust mõõdetakse samades ühikutes kui sulamissoojustki – džaulides kilogrammi kohta (1 J/kg)
Keemistemperatuuril toimuval kondenseerumisel vabaneb sama palju soojust kui kulub sama koguse aine aurustamiseks:
Sublimatsioon-härmatumine
Seega tuleb sublimeerimiseks energiat kulutada, härmatamisel energia vabaneb.
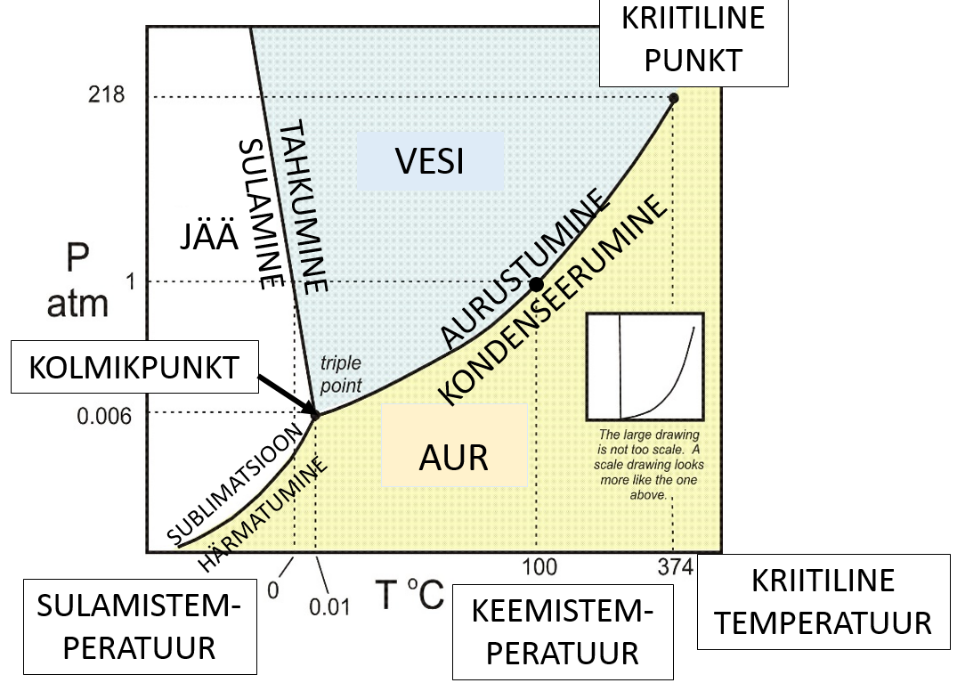
Olekudiagramm
Graafikut, mis kujutab Tp-teljestikus (vabamuutujaks temperatuur, seotud muutujaks rõhk) ühe konkreetse aine erinevaid olekuid ehk faase temperatuuri ja sellega seonduvalt ka rõhu muutumisel, nimetatakse olekudiagrammiks.
Erinevad jooned olekudiagrammi graafikul kujutavad erinevaid faasisiirdeprotsesse. Punkt graafikul kujutab aine vastavalt olekuparameetreid.
Tahket (jää) ja vedelat (vesi) faasi eraldavat joont nimetatakse sulamis/tahkumiskõveraks. Vedelat (vesi) ja gaasilist (aur) faasi eraldavat joont aurustumis/kondenseerumiskõveraks. Tahket (jää) ja gaasilist (aur) faasi eraldab sublimatsiooni/härmatamiskõver.
Sulamis-, sublimatsiooni ja aurustumiskõverate lõikepunkti nimetatakse kolmikpunktiks – selles olekus võib aine korraga esineda kõigis kolmes olekus.
Märkasid viga? Anna sellest teada ja teeme TaskuTarga koos paremaks!