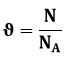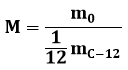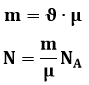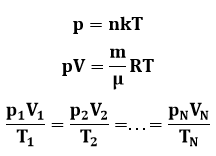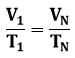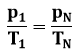Soojusnähtused
Ainehulk:
kus ϑ – ainehulk, N molekulide arv kehas, NA=6,02∙1023 mol-1 – Avogadro arv
Molekulmass:
kus M – molekulmass (ühikuta), m0 – aine molekuli mass (kg); ![]() – süsinik-12 aatomi mass (kg)
– süsinik-12 aatomi mass (kg)
Molaarmassi:
kui μ – molaarmass (kg/mol); NA=6,02∙1023 mol-1 – Avogadro arv; m0 – molekuli mass (kg)
Sulle võivad huvi pakkuda need õppematerjalid:
Eesti keele grammatika kordamine 9. klassile
Õpime tähti. L-täht
Häälikute pikkused
Õpime tähti. B-täht
Õpime tähti. N-täht
Harjuta eesti keelt A2-B1
Õpi eesti keelt teise keelena B2. Lugemine
HANS JA GRETE. Muinasjutt kuulamiseks
Tundetarkus lastele. KURBUS
Õpime tähti. Ä-täht.
Ruutvõrrand
Ruumilised kujundid
Liitmine 20 piires
MEISTERDA! Jõulupuu laua kaunistamiseks
Õpime tähti. E-täht
Harjutamine teeb meistriks: kuhu käib koma?
Ainekoguse mass, osakeste arv selles:
kus m – ainekoguse mass (kg), ϑ – ainehulk (mol), μ – molaarmass (kg/mol), N – osakeste arv ainekoguses, NA=6,02∙1023 mol-1 – Avogadro arv
Ideaalgaasi molekulide keskmine kineetiline energia (temperatuuri definitsioonvalem):
kus ![]() – gaasimolekulide keskmine kineetiline energia = molekulide kineetiliste energiate aritmeetiline keskmine (J), k = 1,3806578∙10-23 J/K ≈ 1,38∙10-23 J/K – Boltzmann’i konstant ning T – keha temperatuur (K).
– gaasimolekulide keskmine kineetiline energia = molekulide kineetiliste energiate aritmeetiline keskmine (J), k = 1,3806578∙10-23 J/K ≈ 1,38∙10-23 J/K – Boltzmann’i konstant ning T – keha temperatuur (K).
Ideaalse gaasi rõhk:
kus: p – ideaalse gaasi poolt anuma seintele avaldatav rõhk (Pa), n – molekulide kontsentratsioon (m-3) – n=N/V (N – osakeste arv anumas; V – anuma ruumala – m3), ![]() – molekulide ruutkeskmine kiirus (m2/s2).
– molekulide ruutkeskmine kiirus (m2/s2).
Ideaalse gaasi olekuvõrrand:
kus p – gaasi rõhk (Pa), n – osakeste kontsentratsioon (n-3), T – gaasi temperatuur (K), k = 1,38∙10-23 J/K – Boltzmann’i konstant, V – gaasi ruumala (m3), m – gaasi mass (kg), μ – gaasi molaarmass (kg/mol), R = NA∙k = 8,314510 J/(mol∙K) ≈ 8,31 J/(mol∙K) – universaalne gaasikonstant; p1, V1, T1 – on gaasi rõhk, ruumala ja temperatuur ühes olekus, pN, VN ja TN – aga sama gaasikoguse rõhk, ruumala ja temperatuur mingis teises olekus.
Boyle’ – Mariotte’i seadus (isotermiline protsess):
kus p1, V1,– on gaasi rõhk (Pa), ruumala (m3) ühes olekus, p2, V2, – aga sama gaasikoguse rõhk ja ruumala mingis teises olekus.
Charles’i seadus (isohooriline protsess):
kus V1, T1,– on gaasi ruumala (m3) ja temperatuur (K) ühes olekus, VN, TN – aga sama gaasikoguse temperatuur ja ruumala mingis teises olekus.
Gay-Lussac’i seadus (isobaariline protsess):
kus p1, T1,– on gaasi rõhk (Pa) ja temperatuur (K) ühes olekus, pN, TN – aga sama gaasikoguse rõhk ja temperatuur mingis teises olekus.
Märkasid viga? Anna sellest teada ja teeme TaskuTarga koos paremaks!