ELEKTRONSKEEM
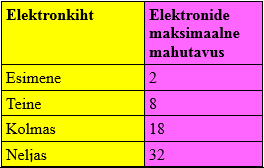
Iga elemendi aatomil on vaid talle omane elektronkatte ehitus, mis oleneb perioodist ja rühmast, kus ta asub. Esimeses perioodis asuvatel elementide aatomitel on ainult üks elektronkiht, kus saab maksimaalselt olla kaks elektroni. Elektronkihtide loendamist alustatakse tuumale kõige lähemal asuvast kihist ja tuumast kõige kaugemal asetsevat kihti nimetatakse väliseks elektronkihiks. Esimese perioodi elementide ainus elektronkiht on seega ühtlasi ka väliselektronkiht. Teise perioodi elementide aatomitel on kaks elektronkihti, kuhu mahub kokku maksimaalselt 10 elektroni. Elektronid, mis ei mahu esimesse ära, lähevad järgmisse kihti. Kolmanda perioodi elementidel on kolm elektronkihti ning sinna mahub kokku maksimaalselt 18 elektroni ( esimesse max. 2, teise max. 8, kolmandasse ehk viimasesse max.8).
Sulle võivad huvi pakkuda need õppematerjalid:
Jäätmed pole kõigest prügi
Loodusõpetuse tööraamat 3. klassile
Elektronskeem on elektronkatte kujutamise viis, mis näitab elektronkihte ja nendel asuvaid elektrone kasutades selleks elemendi tähist, sulgusid ja numbreid.
Näidisülesanne:
Kloori (Cl) aatominumber on 17, mis tähendab, et kloori aatomis on 17 prootonit ja 17 elektroni.
– Märgime esmalt kloori tähise ja selle järgi tema tuumalaengu: Cl: +17
– Järgmisena peame paigutama kihtidena ära 17 elektroni. Kuna kloor asub kolmandas perioodis, siis on tal järelikult kolm elektronkihti. Esimesel kihil on alati maksimaalselt 2 elektroni. Märgimegi selle skeemi ära. Cl: +17| 2)
– Paigutamata on veel 17 – 2= 15 elektroni. Teame, et teine kiht mahutab maksimaalselt 8 elektroni. Seega võimegi skeemile kanda teise kihi tema 8 elektroniga.
Cl: +17| 2)8). Nüüd on ära paigutatud 10 elektroni.
– Kolmandal kihil võib kõige rohkem olla 18 elektroni, kuid kuna antud juhul on kolmas kiht ühtlasi ka viimane, siis võib seal olla maksimaalselt kaheksa elektroni. Kuna meil on veel paigutada 17-10= 7 elektroni, siis on lõplik elektronskeem: Cl: +17| 2)8)7). Kuna Cl asub VIIA rühmas, siis peakski tema välises kihis olema 7 elektroni, seega olema elektronskeemi õigesti koostanud.
TESTID:
RISTSÕNA:
Märkasid viga? Anna sellest teada ja teeme TaskuTarga koos paremaks!