Keemiline vooluallikas – galvaanielement
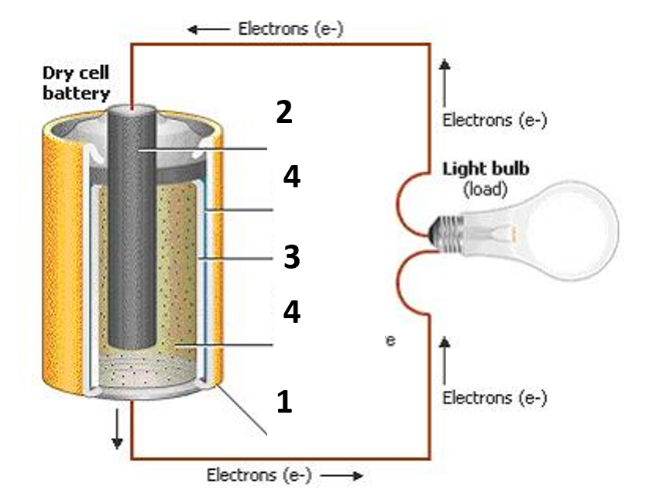
Kõige lihtsam keemiline vooluallikas – galvaanielement koosneb järgmistest osadest:
(1) ümbritsev, enamasti tsingist kest, mis on tavaliselt ka vooluallika negatiivseks pooluseks
(2) vaskelektrood, mis on vooluallika positiivseks pooluseks
(3) poorne vahesein, mis laseb endast läbi ioone ja elektrone, aga mitte lahuseid
(4) elektrolüüt – enamasti on teine teisel pool vaheseina erineva soola vesilahus.
Elektrolüüdis asuvad metallid hakkavad elektrolüüdis lahustuma. Tulemuseks on vabade elektronide positiivsete tsingiioonide tekkimine lahuses. Siin tuleb märkida, et lahusesse lisandub tsinkelektroodilt ainult tsingiioone, vaseioonid on vastavas lahuses juba iseenesest olemas, neid vaskelektroodilt juurde ei teki. Vaskelektroodil toimub hoopis vaseioonide välja sadestumine – ioon liidab endaga vajalikul arvul elektrone, muundub aatomiks ning sadestub.
Sulle võivad huvi pakkuda need õppematerjalid:
Funktsioonide graafikud
Ruutjuur, tehted ruutjuurtega
Lahutamine 20 piires
Harjuta eesti keelt A2-B1. Grammatika
Liitmine 10 piires
Reesi Kuslap ja Kristiine Kurema. Kuidas õhinaga õpetada ehk mismoodi innustada õpilasi õppima?
Silbitamine algklassidele
Aatomid ja molekulid
VAHVA RÄTSEP. Muinasjutt kuulamiseks
I ja J-i õigekiri
Ioonid
Kirjalik liitmine
Numbrilised seosed
Tänu ühel pool vaheseina toimuvale ioonide lisandumisele ja teisel pool seina toimuvale sadestumisele, tekibki elektroodide laengute erinevus – tsinkelektroodist saab vooluallika negatiivne poolus, vaskelektroodist aga positiivne.
Keemiliste reaktsioonide tulemusena tekib elemendis (sise)energia ülejääk, mis muundubki elektrienergiaks.
Taoline protsess saab kesta seni, kuni soolalahusel on piisavalt võimekust uusi tsinkioone tekitada. Kui võimekus kaob, lakkab galvaanielement töötamast ning tema võimet laenguid eraldada pole võimalik taastada – seepärast öeldakse, et galvaanielemendis toimuvad protsessid on mittepööratavad.