Happed
Happed on liitained, mis koosnevad vesinikust ja happejäägist. Happejäägiks nimetatakse seda rühmitust, mis on happe valemis vesinikuga seotud.
Tuntumad happed on järgmised:
Hapete vesilahustes esinevad happed ioonidena. Happe annab vesilahusesse positiivse vesinikiooni (H+) ning negatiivselt laetud happejäägi (happeaniooni). Happejäägi laeng võrdub vesinike arvuga happe valemis.
Sulle võivad huvi pakkuda need õppematerjalid:
Ионы
Aatomid ja molekulid
Tutvus keemiaga
Знакомство с химией
Атомы и молекулы
Lahused
Ioonid
Растворы
Oksüdatsiooniaste
HCl = H+ + Cl–
H2SO4 = 2H+ + SO42-
Happeid liigitatakse hapnikhapeteks (H2SO4, HNO3) ja hapnikuta hapeteks (HCl, H2S) vastavalt sellele, kas happeanioon sisaldab hapnikku või mitte.
Happe tugevuse järgi saab happeid liigitada tugevateks ja nõrkades hapeteks. Tugevad happed on HCl, HBr, HI, H2SO4, HNO3. Ülejäänud tuntumad happed on nõrgad happed.
Kõikidele hapnikhapetele vastab ka kindel oksiid, mida nimetatakse happeliseks oksiidiks. Happelises oksiidis on elemendi oksüdatsiooniaste sama, mis temale vastavas oksiidis.
Hapete saamine
Üksvõimalus happeid saada on happelise oksiidi reageerimine veega. Niimoodi on võimalik saada enamus hapnikhappeid.
SO3 + H2O = H2SO4
SO2 + H2O = H2SO3
CO2 + H2O = H2CO3
N2O5 + H2O = 2HNO3
P4O10 + 6H2O = 4H3PO4
Hapnikuta happeid saadakse vastavate gaaside (HCl, H2S) lahustumisel vees.
Hapete omadusi
Happed on söövitava toimega ained. Eriti ohtlikud on tugevad happed, mis riidele (või mõnele muule pinnale) sattudes võivad sinna augu söövitada.
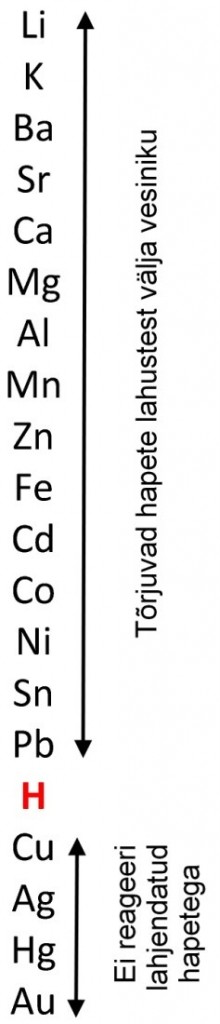
Üheks hapete tähtsamaks omaduseks on reageerimine metallidega. See, kas metall happega reageerib, sõltub metalli aktiivsusest. Väga väikese aktiivsusega metallid nagu vask, hõbe, kuld, hapetega ei reageeri. Metallide rida, kus metallid on paigutatud ritta aktiivsuse kahanemise järgi nimetatakse metallide pingereaks (vt joonis).
Metalli reageerimisel happega tõrjub metall happest välja vesiniku ning tekib uus ühend sool (metall ja happeanioon ühinevad).
Ca + H2SO4 = CaSO4 + H2
Sellist keemilist reaktsiooni, mille käigus liht- ja liitaine ühinemisel tekivad uued liht- ja liitained nimetatakse asendusreaktsiooniks.
Metalli reageerimine hapetega on redoksreaktsioon, kus metall käitub alati redutseerijana ning vesinikuioonid on oksüdeerijad.
Need metallid, mis paiknevad metallide pingereas vesinikust paremal lahjendatud hapetega ei reageeri.
Ag + HCl → reaktsiooni ei toimu
Erandiks on lämmastikhape (nii lahjendatud kui kontsentreeritud) ning kontsentreeritud väävelhape. Nende hapetega võivad reageerida ka need metallid, mis on vesinikust paremal, kuid selle reaktsiooni käigus vesinikku ei teki, vaid eralduvad muud ained.
Cu + 4HNO3 = Cu(NO3)2 + 2NO2 + 2H2O
Lisainfo
Märkasid viga? Anna sellest teada ja teeme TaskuTarga koos paremaks!