Ainete lahustumisprotsess
Ainete lahustumisel vedelikes (peamiselt vees) toimub aineosakeste seostumine vedeliku (vee) osakestega. Kuna peamiseks lahustiks, mida lahuste valmistamisel kasutatakse on vesi, siis on kõik näited ja seletused toodud vee põhjal.
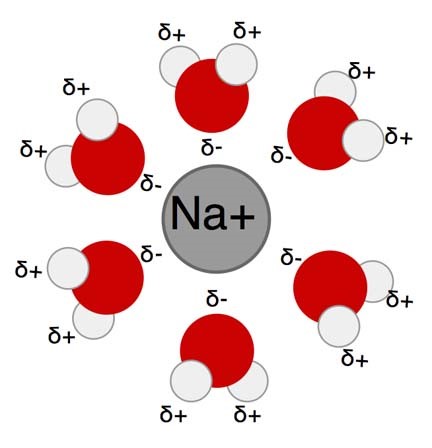
Soolade, hapete või aluste lahustumisel vees toimub nende ainete lagunemine ioonideks. Seda protsessi nimetatakse elektrolüütiliseks dissotsiatsiooniks. Aine (näiteks NaCl) laguneb vees Na+ ja Cl– ioonideks. Aine lagunemine toimub seetõttu, et vee molekulid tungivad soola kristallvõresse ning lagundavad kristallvõre. Lahusesse läinud ioonid on seostunud (ümbritsetud) vee molekulidega. Seda nähtust, kus vee molekulid seostuvad aine osakestega nimetatakse hüdraatumiseks ning tekkinud ioone hüdraatunud ioonideks.
Sulle võivad huvi pakkuda need õppematerjalid:
Ioonid
Растворы
Ионы
Tutvus keemiaga
Oksüdatsiooniaste
Знакомство с химией
Aatomid ja molekulid
Атомы и молекулы
Lahused
Happed lagunevad samamoodi ioonideks nagu soolad ning tekkinud ioonid on samuti ümbritsetud vee molekulidega. Lahusesse läinud vesinikioon (H+) vesilahuses üksikult ei esine, vaid ta on alati seostunud ühe vee molekuliga ning lahuses esineb ta H3O+ iooninda – hüdrooniumioonina. Võrrandites me kirjutame siiski vesinikiooni lihtsuse mõttes H+.
VIDEOD:
Lahused (ing)
Lisainfo
Märkasid viga? Anna sellest teada ja teeme TaskuTarga koos paremaks!