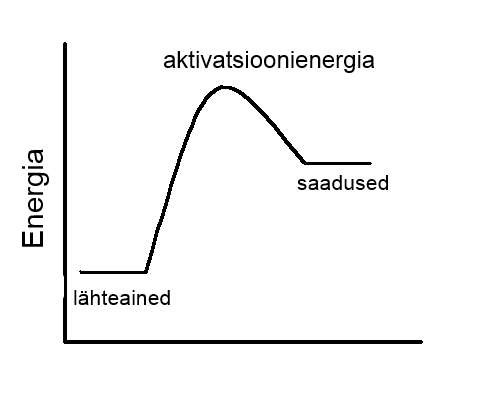
Ekso- ja endotermilised reaktsioonid
Keemiliste reaktsioonide käigus toimub alati energia eraldumine või neeldumine. Neid reaktsioone, mille käigus energia eraldub nimetatakse eksotermilisteks reaktsioonideks ning neid reaktsioone, mille käigus energia neeldub nimetatakse endotermilisteks reaktsioonideks.
Keemilise reaktsiooni käigus alati katkevad lähteainete osakeste vahelised sidemed ning tekivad uued keemilised sidemed. Sideme katkemiseks alati kulub energiat ning sideme tekkimisel eraldub energiat. Seda, kas reaktsioonil eraldub või neeldub energiat, sõltub sellest, kas ülekaalus on sideme katkemisel kulunud energia või sideme tekkimisel eraldunud energia.
Sulle võivad huvi pakkuda need õppematerjalid:
Lahused
Tutvus keemiaga
Растворы
Ioonid
Знакомство с химией
Aatomid ja molekulid
Oksüdatsiooniaste
Атомы и молекулы
Ионы
Ühinemisreaktsioonid on enamasti eksotermilised reaktsioonid, kuna nendes reaktsioonides on ülekaalus sideme tekkimisel eraldunud energia. Eksotermiline reaktsioon on alati ka põlemine.
Lagunemisreaktsioonid on enamasti endotermilised, kuna nendes reaktsioonides kulub sideme lõhkumiseks rohkem energiat, kui tekib uute sidemete tekkimisel.
Loomulikult esineb ka erandeid, kus ühinemisreaktsioon võib olla endotermiline ning lagunemisreaktsioon eksotermiline. Näiteks on eksotermiline ammooniumdikromaadi lagunemine.
Reaktsiooni soojusefekti iseloomustab reaktsiooni entalpiamuut ΔH. Entalpiamuutu saab arvutada lähteainete ja saaduste tekkeentalpiate järgi.
entalpiamuut ΔH = Saaduste tekkeentalpia – lähteainete tekkeentalpia
Tekkeentalpia näitab seda energiat, mis kulub või eraldub aine tekkimisel lihtainetest. Lihtainete tekkeentalpia on alati null.
Eksotermilise reaktsiooni entalpiamuut ΔH < 0 ning endotermilise reaktsiooni ΔH > 0. See tuleneb entalpiamuudu arvutamise valemist. Kui saaduste energia on väiksem kui lähteainete energia, siis reaktsiooni käigus eraldub energiat (ΔH < 0) ning tegemist on eksotermilise reaktsiooniga.
Ekso- ja endotermilised reaktsioonid (ing)
Sideme energia (ing)
Reaktsiooni entalpia (ing)
Reaktsiooni entalpia 2 (ing)
Lisainfo
Märkasid viga? Anna sellest teada ja teeme TaskuTarga koos paremaks!