Aatomi ehitus
Aatomi osakesed
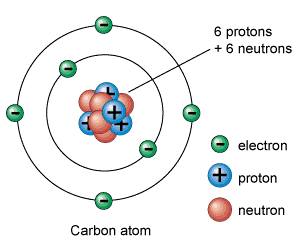
Aatom koosneb aatomituumast ning elektronkattest. Aatomituum omakorda koosneb prootonitest ja neutronitest. Prooton on positiivse laenguga osake ning neutron on laenguta osake. Prootoni laeng on arvuliselt võrdne elektroni laenguga, ainult märgilt vastupidine. Elektroni laengut nimetatakse elementaarlaenguks, kuna see on looduses esinev väikseim laeng.
Sulle võivad huvi pakkuda need õppematerjalid:
Знакомство с химией
Атомы и молекулы
Ионы
Ioonid
Lahused
Oksüdatsiooniaste
Tutvus keemiaga
Растворы
Aatomid ja molekulid
Tänapäeval on teada, et prootonid ja neutronid koosnevad omakorda veel väiksematest osakestest – kvarkidest. Leitud on kuut erinevat liiki kvarke, kuid prootonid ja neutronid koosnevad kahte liiki kvarkidest – u- ja d-kvarkidest. Prootoni neutroni laengud tulenevadki kvarkide laengutest.
Elektronkate koosneb elektronidest, mis on jaotunud elektronkihtidele. Elektrone iseloomustab eriline omadus, mis seostub nende sisemise liikumisega – spinn. Piltlikult öeldes näitab spinn elektronide pöörlemist. Kvantfüüsikas on elektroni spinni väärtuseks ![]() või
või ![]() . Elektronid paiknevad elektronkihtidel paarikaupa, kusjuures erineva spinniga elektronid moodustavad püsiva süsteemi – elektronpaari.
. Elektronid paiknevad elektronkihtidel paarikaupa, kusjuures erineva spinniga elektronid moodustavad püsiva süsteemi – elektronpaari.
Aatomit iseloomustavad suurused
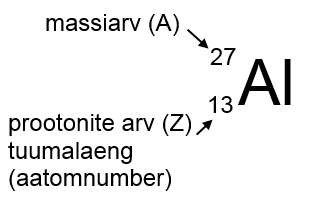
Aatomi kirjeldamiseks on kõige olulisem suurus prootonite arv (tähistatakse tähega Z), mis määrab ära aatomi tuumalaengu ning selle, millise elemendiga on tegemist. Tuumalaengut nimetatakse mõnikord ka aatomnumbriks või järjenumbriks.
Neutronite arvu tähistatakse tähega N ning neutronite ja prootonite koguarvu nimetatakse massiarvuks. Nimetus tuleneb sellest, aatomile annavad massi just prootonid ja neutronid, elektronid. Massiarvu tähistatakse tähega A.
A = Z + N
Teades aine massiarvu ja prootonite arvu saab arvutada neutronite arvu aatomituumas. Näiteks alumiiniumi aatomnumber on 13 ning tema massiarv on 27. Seega on alumiiniumi aatomituumas 27 – 13 = 14 neutronit.
Kuna aatomituumas saab olla täisarv prootoneid ja neutroneid, siis peab ka massiarv olema täisarv. Perioodilisustabelist aga leiame enamike aatomite juurest aga murdarvulisi massiarve. Põhjus on selles, et looduses võib ühe elemendi aatomituuma koostises olla erinev arv neutroneid. Ühe ja sama keemilise elemendi erineva massiarvuga (erineva neutronite arvuga) aatomeid nimetatakse isotoopideks. Perioodilisustabelis antakse massiarvuks erinevate looduslike isotoopide suhteline aatommass, mistõttu see võibki tulla murdarvuline. Näiteks esineb looduses kloori massiarvuga 35 (17 prootonit ja 18 neutronit) ning massiarvuga 37 (17 prootonit ja 20 neutronit). Looduses on 35Cl sisaldus 75% ning 37Cl sisaldus 25% mis annabki nende suhteliseks aatommassiks 35,5.
TEST:
Aatomi ehitus. Leia õiged vastused
VIDEOD:
Ained ja molekulid (ing)
Aatommass, aatomnumber, isotoobid (ing)
Lisainfo
Märkasid viga? Anna sellest teada ja teeme TaskuTarga koos paremaks!