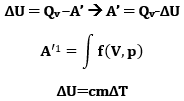- Kopeeri link
- Jaga Stuudiumis
- Teata veast
Termodünaamika I printsiip ja isoprotsessid
Milline gaasiga toimuv soojuslik protsess on gaasi töö seisukohalt kõige kasulikum?
Kui gaas teeb tööd, siis muutub tema siseenergia, gaasi siseenergiat võib muuta ka soojusülekanne (kui gaas soojeneb või jahtub väliskeskkonnaga kokkupuutes):
1 Tähistame taoliselt graafilise integreerimise teel leitavat suurust – gaasi tööd A’ seosest, kus gaasi ruumala V on vabamuutuja ning rõhk p seotud muutuja.
Sulle võivad huvi pakkuda need õppematerjalid:
Tundetarkus lastele. VIHA
Õpi eesti keelt teise keelena B2
Liitmine 20 piires
Protsendid põhikooli matemaatikas
Protsendi rakendused igapäevaelus
Ruumilised kujundid
Õpime tähti. L-täht
I ja J-i õigekiri
Harjuta eesti keelt A2-B1. Mängi ja nuputa
Õpime tähti. N-täht
Väike protsendiamps
Eeldame, et gaas saab kõigis isoprotsessides väliskeskkonnalt ühesuguse soojushulga Qv.
Isohoorilises protsessis gaas ei paisu – järelikult ei tee gaas saadava soojuse arvelt tööd, kogu gaasile antav energia läheb gaasi temperatuuri (siseenergia) suurendamiseks => Qv = ΔU = cmΔT
Isobaarilises protsessis on gaasi temperatuur võrdeline ruumalaga, seega gaasi temperatuuri suurenemisel (siseenergia suurenemisel) gaas paisub. Paisumisel teeb gaas aga tööd. Isobaarilistes protsessides jaguneb gaasile antav soojus siseenergia suurenemise (temperatuuri tõusuks vajaliku) ning töö gaasi poolt tehtava tööks (ruumala suurenemise ehk paisumise) vajaliku energiakoguse vahel. Nii muutubki isobaarilise protsessi käigus gaasi tööks ainult osa gaasile antud soojusest => Q = A’ + cmΔT
Kuna gaasi siseenergia sõltub temperatuurist, siis isotermilise protsessi korral, kus gaasi temperatuur protsessi vältel ei muutu, ei muutu ka gaasi siseenergia. Kui isotermilises protsessis gaas paisub, siis läheb kogu soojus gaasi tööks => Q = A’
Seega gaas teeb kõige rohkem tööd isotermilise paisumise korral.
Märkasid viga? Anna sellest teada ja teeme TaskuTarga koos paremaks!