- Kopeeri link
- Jaga Stuudiumis
- Teata veast
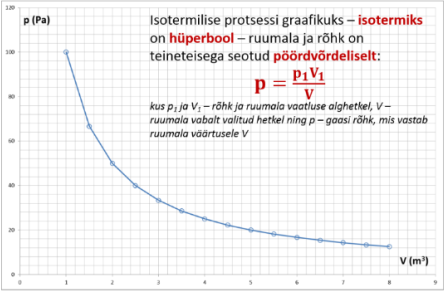
Isotermiline protsess
Kui protsessi käigus ei muutu ideaalse gaasi temperatuur, nimetatakse seda isotermiliseks protsessiks.
Kuna protsessi käigus jääb temperatuur samaks ehk T1 = TN, siis võtab isotermilist protsessi kirjeldaval ideaalse gaasi olekuvõrrand kuju:
Seda avaldist tuntakse ka kui Boyle’ – Mariotte’i seadusena, kes on vastavalt inglise ja prantsuse teadlased, kes nimetatud seaduspärasuse teineteisest sõltumatult avastasid.
Sulle võivad huvi pakkuda need õppematerjalid:
Liitmine ja lahutamine 10 piires
Eesti keele grammatika kordamine 9. klassile
Tundetarkus lastele. RÕÕM
Funktsioonide graafikud
Harjuta eesti keelt A2-B1. Lugemine
Väike protsendiamps
Geomeetria
Üksliikmed, hulkliikmed ja tehted nendega
Tundetarkus lastele. PÕHIEMOTSIOONID
Harjuta eesti keelt A2-B1. Kuulamine
Растворы
Urme Raadik ja Sille Jõgeva. Omavahelised suhted
VAPPER TINASÕDUR. Muinasjutt kuulamiseks
Tasandilised kujundid
Seadusest nähtub, et kui jääval temperatuuril gaasi kokku suruda (ruumala väheneb), siis suureneb gaasi rõhk, kui aga gaas paisub jääval temperatuuril, siis rõhk väheneb.
Isotermiliseks võime lugeda protsessi, mis toimub auto sisepõlemismootorites, kui kütusesegu plahvatab ning seejärel kiiresti paisub, liigutades samal ajal silindris liikuvat kolbi. Isotermilisi protsesside kasutataksegi peamiselt gaaside siseenergia muutmisel mehaaniliseks tööks.
Märkasid viga? Anna sellest teada ja teeme TaskuTarga koos paremaks!